 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
根据下列各组配离子化学式后面括号内所给出的条件,确定它们各自的中心离子的价层电子排布和配
(1)[Mn(C2O4)3]3-(高自旋),[Mn(CN)6]3-(低自旋);
(2)[Fe(en)3]3+(高自旋),[Fe(CN)6]3-(低自旋);
(3)[CoF6]3-(高自旋),[Co(en)3]3+(低自旋)
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码进入小程序
拍照、语音搜题,请扫码进入小程序
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
(1)[Mn(C2O4)3]3-(高自旋),[Mn(CN)6]3-(低自旋);
(2)[Fe(en)3]3+(高自旋),[Fe(CN)6]3-(低自旋);
(3)[CoF6]3-(高自旋),[Co(en)3]3+(低自旋)
 答案
答案
 更多“根据下列各组配离子化学式后面括号内所给出的条件,确定它们各自的中心离子的价层电子排布和配”相关的问题
更多“根据下列各组配离子化学式后面括号内所给出的条件,确定它们各自的中心离子的价层电子排布和配”相关的问题
第1题
画出下列配离子的电子排布式,指出杂化轨道的名称及配离子的空间构型。
(A)外轨型:[CuCl2]-,[AIF6]3-,[NiCl2(NH3)2];
(B)内轨型:[Pt(NH3)4]2+,[Pt(CN)4]2-。
第4题
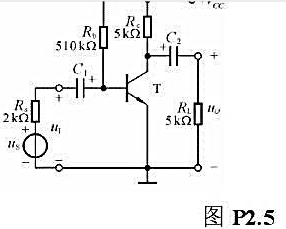
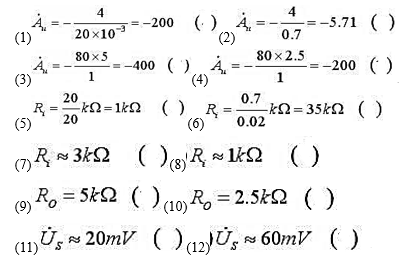
第6题
计算下列水溶液的pH(括号内为pKa).
(1)0.10mol·L-1乳酸和0.10mol·L-1乳酸钠(3.76);
(2)0.01mol·L-1邻硝基酚和0.012mol·L-1邻硝基酚的钠盐(7.21)
(3)0.12mol·L-1氯化三乙基胺和0.01mol·L-1三乙基胺(7.90);
(4)0.07mol·L-1氯化丁基胺和0.06mol·L-1丁基胺(10.71).
第7题
第10题:该公司所制定的到2010年的人力资源规划是一种()
A.战术性人力资源计划
B.人员招聘计划
C.战略性人力资源计划
D.年度人力资源计划
第8题
A.凡使用商品名的中药制剂,必须在商品名下方的括号内标明法定通用名称等
B.药品说明书和标签的文字表述应当科学、规范、准确
C.药品说明书和标签中的文字应当清晰易辨,标识应当清楚醒目,不得有印字脱落或者粘贴不牢等现象,不得以粘贴、剪切、涂改等方式进行修改或者补充
D.不得夹带其他任何介绍或者宣传产品、企业的文字、音像及其他资料
第10题
(2)从书中查出上述各碳酸盐的分解温度(CdCO3为345℃),与计算结果加以比较,并加以评价.
(3)各碳酸盐分解温度的实验值与由计算结果所得出的有关碳酸盐的分解温度的规律是否一致?并从离子半径、离子电荷、离子的电子构型等因素对上述规律加以说明.
(3)分解温度的实际值和计算值的规律是一致的.金属离子的半径越小,离子所带的电荷数越大,极化能力就越强,相应碳酸盐分解温度越低;金属离子电子构型为18e的极化能力比8e的强;而极化越大,相应的碳酸盐越易分解.